Ficin für Proteinhydrolyse: Fehlerbehebung bei Dosierung, pH und Temperatur
Optimieren Sie ficin für die Proteinhydrolyse mit praxisnahen Hinweisen zu Dosierung, pH, Temperatur, QC, Pilotvalidierung und Lieferantenqualifizierung.

Für Hersteller, die das Ficin-Enzym für die Proteinhydrolyse bewerten, hängt die Prozessleistung davon ab, Enzymaktivität, Substrat, pH, Temperatur, Verweilzeit und nachgelagerte Kontrollen aufeinander abzustimmen.
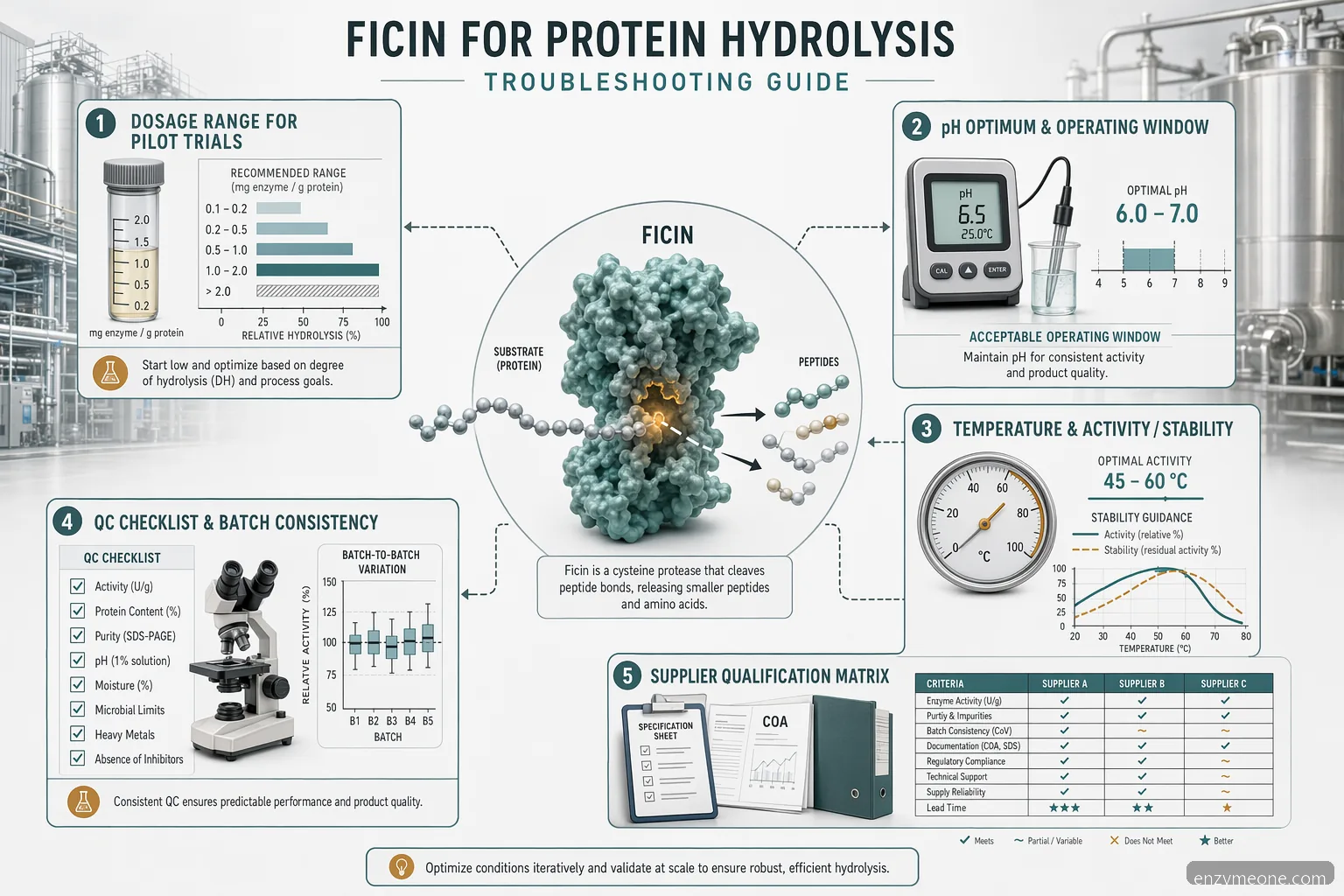
Warum Ficin sich bei der Proteinhydrolyse anders verhält
Ficin ist eine pflanzlich gewonnene Protease, die häufig mit Feigenlatex in Verbindung gebracht wird, daher suchen Käufer möglicherweise auch nach Feigenenzym für die Proteinhydrolyse. In industriellen Systemen wird es eingesetzt, um Proteinsubstrate in kleinere Peptide zu spalten, die Löslichkeit zu verbessern, die Textur zu modifizieren oder die Herstellung funktioneller Inhaltsstoffe zu unterstützen. Die Leistung kann je nach Substrat, Vorbehandlung, Salzgehalt, Feststoffgehalt und der Aktivitätsmethode des Lieferanten variieren. Eine Dosierung, die bei Kollagen, Fleischabschnitten, pflanzlichem Protein oder Gelatine funktioniert, lässt sich nicht ohne Weiteres auf Milchprodukte, Meeresfrüchte oder gemischte Proteinströme übertragen. Für die Fehlerbehebung sollten Sie klären, ob das Ziel eine schnelle Viskositätsreduktion, eine kontrollierte Peptidgröße, eine verbesserte Löslichkeit, Geschmacksentwicklung oder eine Ausbeutesteigerung ist. Jedes Ziel kann einen anderen Endpunkt und einen anderen Enzyminaktivierungsschritt erfordern. Die industrielle Proteinhydrolyse mit Ficin sollte daher zunächst im Labormaßstab entwickelt und anschließend unter denselben Misch-, Heiz- und Haltebedingungen validiert werden, die auch im Produktionsmaßstab zu erwarten sind.
Definieren Sie den gewünschten Hydrolyse-Endpunkt, bevor Sie die Dosierung auswählen. • Vergleichen Sie Lieferanten anhand von Enzymaktivität und Anwendungsleistung. • Validieren Sie am realen Substrat, nicht nur an Modellproteinen.
Ausgangsdosierungen für Pilotversuche
Bei Ficin für die Proteinhydrolyse sollte die Dosierung möglichst in Aktivitätseinheiten pro Kilogramm Protein oder Substrat angegeben werden, sofern der Ficin-Enzymlieferant für die Proteinhydrolyse eine validierte Aktivitätsmethode bereitstellt. Wenn nur eine prozentuale Zugabe verfügbar ist, nutzen Sie diese als Screening-Referenz und rechnen Sie nach Erhalt des COA um. Ein praxisnaher Pilotbereich liegt häufig bei 0.02% bis 0.50% Enzymprodukt bezogen auf das Substratgewicht, abhängig von Aktivitätskonzentration, Proteinzugänglichkeit, Feststoffgehalt, Zeit und gewünschtem Hydrolysegrad. Niedrige Dosierungen können für Texturmodifikation oder milde Solubilisierung geeignet sein, während höhere Dosierungen für zäheres Bindegewebe oder hochfeste Slurries erforderlich sein können. Gehen Sie nicht davon aus, dass mehr Enzym immer die Einsatzkosten senkt. Eine Überhydrolyse kann Bitterkeit erhöhen, die funktionelle Struktur verringern, Filtrationsprobleme verursachen oder zusätzliche Korrekturschritte im Downstream erfordern. Erstellen Sie eine Dosierungskurve mit mindestens drei Enzymstufen und einer Kontrolle ohne Enzym.
Testen Sie niedrige, mittlere und hohe Dosierungen unter identischen Bedingungen. • Normalisieren Sie die Ergebnisse möglichst auf Aktivitätseinheiten. • Bewerten Sie die Kosten pro Kilogramm des fertigen Hydrolysats, nicht nur den Einkaufspreis.
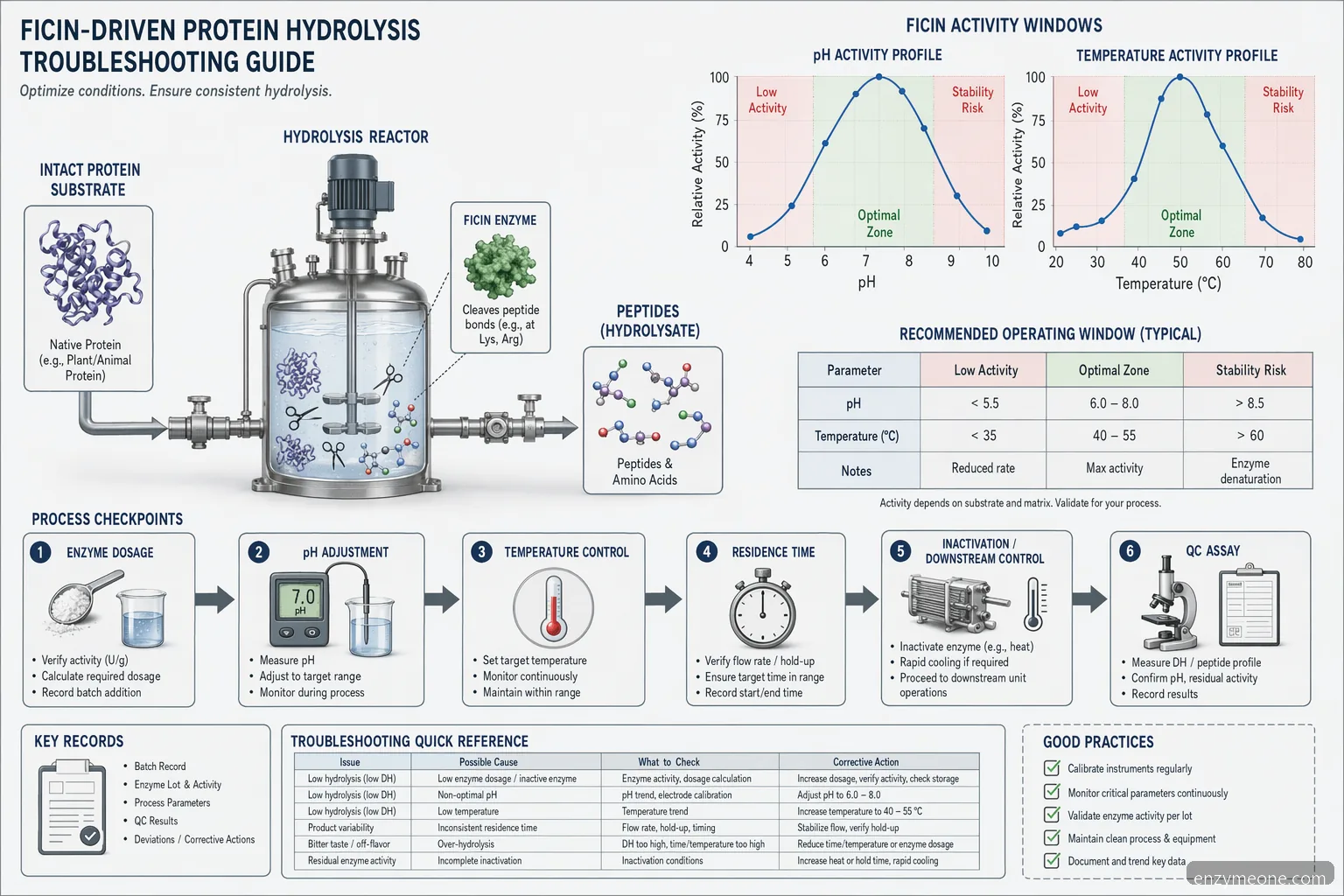
Fehlerbehebung bei pH und Temperatur
Ficin arbeitet typischerweise am besten in leicht sauren bis nahezu neutralen Prozessfenstern, der ideale pH-Wert muss jedoch anhand des TDS des Lieferanten und des tatsächlichen Substrats bestätigt werden. Ein gängiger Screening-Bereich liegt bei pH 5.0 bis 7.5, mit anschließender engerer Optimierung, sobald löslicher Stickstoff und die Peptidverteilung gemessen werden. Die Temperatursuche beginnt häufig bei 40°C bis 60°C. Niedrigere Temperaturen können empfindliche Aromen schützen oder das mikrobiologische Risiko in Kombination mit kurzen Haltezeiten reduzieren, während höhere Temperaturen die Reaktionsgeschwindigkeit verbessern können, bis die Enzymstabilität nachlässt. Wenn die Hydrolyse stagniert, prüfen Sie pH-Verschiebungen durch Pufferwirkung des Substrats, Säurezugabe, Mineralsalze oder freigesetzte Aminogruppen. Wenn die Leistung nach der Skalierung abnimmt, verifizieren Sie Aufheizzeit, Tankgradienten, Scherung und die tatsächliche Produkttemperatur statt nur die Manteltemperatur. Für eine kontrollierte Produktion sollten sowohl die aktive Hydrolysetemperatur als auch die thermische Inaktivierungsbedingung definiert werden, mit der die Reaktion gestoppt wird.
Erster pH-Screeningbereich: typischerweise pH 5.0 bis 7.5. • Erster Temperatur-Screeningbereich: typischerweise 40°C bis 60°C. • Bestätigen Sie die Endwerte mit dem TDS des Lieferanten und mit Werksversuchen. • Dokumentieren Sie die Enzyminaktivierung, um eine weitere Hydrolyse zu verhindern.
QC-Prüfungen, die Chargenschwankungen verhindern
Die industrielle Proteinhydrolyse mit Ficin erfordert analytische Kontrollen, die über Aussehen und Ausbeute hinausgehen. Erfassen Sie den pH-Wert vor der Zugabe, während der Haltezeit und am Endpunkt. Messen Sie die Temperatur an repräsentativen Stellen des Tanks. Je nach Produkt können zur QC der Hydrolysegrad, löslicher Stickstoff, freier Aminostickstoff, Peptid-Molekulargewichtsverteilung, Viskosität, Trübung, Filtrationsrate, Feuchte, Asche, mikrobiologische Indikatoren und sensorische Merkmale wie Bitterkeit oder Schwefelnote gehören. Für die Fehlerbehebung sollten Proben aus jedem Zeitpunkt aufbewahrt und mit einer historisch akzeptierten Charge verglichen werden. Ist eine Charge unzureichend hydrolysiert, prüfen Sie Enzymlagerung, Lot-Aktivität, Dosiergenauigkeit, Mischen, Verweilzeit und die Vorbehandlung des Substrats. Ist eine Charge überhydrolysiert, reduzieren Sie Haltezeit, Dosierung oder Temperatur und bestätigen Sie den Inaktivierungsschritt. Eine praxisgerechte Spezifikation sollte sowohl Prozessparameter als auch funktionelle Ergebnisse des Endprodukts enthalten, da derselbe Hydrolysegrad je nach Substrat unterschiedlich ausfallen kann.
Verwenden Sie bei der Skalierung Zeitpunktsproben. • Bewahren Sie Rückstellmuster von akzeptierten und abgelehnten Chargen auf. • Verknüpfen Sie QC-Ergebnisse mit der funktionellen Leistung, nicht nur mit chemischen Werten.
Wie man einen Ficin-Lieferanten qualifiziert
Ein qualifizierter Ficin-Lieferant für die Proteinhydrolyse sollte für jede Charge ein aktuelles COA, ein TDS mit Aktivitätsdefinition und empfohlenen Einsatzbedingungen sowie ein SDS für den sicheren Umgang bereitstellen. Käufer sollten fragen, wie die Aktivität gemessen wird, ob das Produkt pulverförmig oder flüssig ist, welche Lagerbedingungen empfohlen werden, wie die Trägerzusammensetzung aussieht, welche Allergen- und regulatorischen Informationen für den Markt relevant sind und welche Haltbarkeit zu erwarten ist. Da Aktivitätsassays unterschiedlich sein können, vergleichen Sie Lieferanten in Ihrem eigenen Substratsystem und nicht nur anhand der Deklaration. Fordern Sie Pilotmengen beim Feigenenzym-Lieferanten für die Proteinhydrolyse an und führen Sie Parallelversuche gegen Ihr aktuelles Prozessziel durch. Die Lieferantenbewertung sollte Chargenkonstanz, Reaktionsgeschwindigkeit bei Dokumentationsanfragen, Lieferzeit, Verpackungseignung, technischen Support und Einsatzkosten umfassen. Die beste Wahl ist nicht immer der niedrigste Stückpreis, sondern das Enzym, das den erforderlichen Hydrolyse-Endpunkt im kommerziellen Maßstab zuverlässig erreicht.
Fordern Sie COA, TDS, SDS und Chargenrückverfolgbarkeit an. • Bestätigen Sie Aktivitätsmethode und Lageranforderungen. • Führen Sie vor der kommerziellen Freigabe Parallel-Pilotversuche durch. • Berechnen Sie die Einsatzkosten anhand der tatsächlichen Endpunktleistung.
Technische Einkauf-Checkliste
Fragen von Käufern
Ein praxisnaher Screeningbereich liegt häufig bei 0.02% bis 0.50% Enzymprodukt bezogen auf das Substratgewicht, die bessere Grundlage sind jedoch Aktivitätseinheiten pro Kilogramm Protein oder Substrat. Führen Sie eine Dosierungskurve mit mindestens drei Stufen und einer Kontrolle ohne Enzym durch. Wählen Sie die Dosierung, die den erforderlichen Endpunkt bei den niedrigsten verlässlichen Einsatzkosten ohne Überhydrolyse erreicht.
Viele Ficin-Prozesse werden zwischen pH 5.0 und 7.5 gescreent und anschließend anhand des Substrats und des TDS des Lieferanten eingegrenzt. Der beste pH-Wert ist derjenige, der unter realen Produktionsbedingungen das gewünschte Peptidprofil, die Löslichkeit, den Geschmack und die Ausbeute liefert. Überwachen Sie pH-Drift während der Reaktion, da Proteinpufferung und freigesetzte Aminogruppen den effektiven Arbeitspunkt verändern können.
Ein gängiges Pilot-Screeningfenster liegt bei 40°C bis 60°C. Höhere Temperaturen können die Hydrolyserate erhöhen, jedoch nur bis zu dem Punkt, an dem Enzymstabilität oder Produktqualität limitierend werden. Bestätigen Sie die tatsächliche Produkttemperatur im Tank und nicht nur die Mantel-Einstellungen. Sobald der Endpunkt erreicht ist, verwenden Sie einen validierten Inaktivierungsschritt, um weitere Proteolyse zu stoppen und die Chargenkonstanz zu sichern.
Vergleichen Sie Lieferanten anhand der Leistung in Ihrem Substrat, nicht nur nach Preis oder deklarierter Aktivität. Fordern Sie COA, TDS, SDS, Aktivitätsmethode, Lagerbedingungen, Haltbarkeit und Rückverfolgbarkeit an. Führen Sie nach Möglichkeit Parallel-Pilotversuche mit äquivalenten Aktivitätsdosierungen durch. Berechnen Sie anschließend die Einsatzkosten auf Basis von Endpunktzeit, Ausbeute, Filtrationsverhalten, Qualitätsresultaten und Zuverlässigkeit im kommerziellen Maßstab.
Bitterkeit oder ein übermäßiger Viskositätsverlust deuten häufig auf Überhydrolyse, zu hohe Dosierung, lange Verweilzeit, erhöhte Temperatur oder eine verzögerte Inaktivierung hin. Prüfen Sie Zeitpunktsproben, Endpunktdaten und Dosieraufzeichnungen. Ein Korrekturversuch kann die Enzymmenge reduzieren, die Haltezeit verkürzen, die Temperatur senken oder den Stopp-Schritt straffen. Sensorische Prüfungen und Peptidprofil-Analysen können helfen, das akzeptable Betriebsfenster zu bestimmen.
Verwandte Suchthemen
industrielle Ficin-Proteinhydrolyse, industrielle Ficin-Enzym-Proteinhydrolyse, Ficin-Lieferant für Proteinhydrolyse, Ficin-Enzymlieferant für Proteinhydrolyse, Ficin-Enzym für Proteinhydrolyse, industrielle Feigenenzym-Proteinhydrolyse
Ficin for Research & Industry
Need Ficin for your lab or production process?
ISO 9001 certified · Food-grade & research-grade · Ships to 80+ countries
Häufig gestellte Fragen
Welche Dosierung sollten wir für Ficin-Enzym für die Proteinhydrolyse verwenden?
Ein praxisnaher Screeningbereich liegt häufig bei 0.02% bis 0.50% Enzymprodukt bezogen auf das Substratgewicht, die bessere Grundlage sind jedoch Aktivitätseinheiten pro Kilogramm Protein oder Substrat. Führen Sie eine Dosierungskurve mit mindestens drei Stufen und einer Kontrolle ohne Enzym durch. Wählen Sie die Dosierung, die den erforderlichen Endpunkt bei den niedrigsten verlässlichen Einsatzkosten ohne Überhydrolyse erreicht.
Welcher pH-Wert ist für die industrielle Proteinhydrolyse mit Ficin am besten?
Viele Ficin-Prozesse werden zwischen pH 5.0 und 7.5 gescreent und anschließend anhand des Substrats und des TDS des Lieferanten eingegrenzt. Der beste pH-Wert ist derjenige, der unter realen Produktionsbedingungen das gewünschte Peptidprofil, die Löslichkeit, den Geschmack und die Ausbeute liefert. Überwachen Sie pH-Drift während der Reaktion, da Proteinpufferung und freigesetzte Aminogruppen den effektiven Arbeitspunkt verändern können.
Welche Temperatur sollten wir bei Ficin für die Proteinhydrolyse verwenden?
Ein gängiges Pilot-Screeningfenster liegt bei 40°C bis 60°C. Höhere Temperaturen können die Hydrolyserate erhöhen, jedoch nur bis zu dem Punkt, an dem Enzymstabilität oder Produktqualität limitierend werden. Bestätigen Sie die tatsächliche Produkttemperatur im Tank und nicht nur die Mantel-Einstellungen. Sobald der Endpunkt erreicht ist, verwenden Sie einen validierten Inaktivierungsschritt, um weitere Proteolyse zu stoppen und die Chargenkonstanz zu sichern.
Wie vergleichen wir einen Ficin-Lieferanten für die Proteinhydrolyse?
Vergleichen Sie Lieferanten anhand der Leistung in Ihrem Substrat, nicht nur nach Preis oder deklarierter Aktivität. Fordern Sie COA, TDS, SDS, Aktivitätsmethode, Lagerbedingungen, Haltbarkeit und Rückverfolgbarkeit an. Führen Sie nach Möglichkeit Parallel-Pilotversuche mit äquivalenten Aktivitätsdosierungen durch. Berechnen Sie anschließend die Einsatzkosten auf Basis von Endpunktzeit, Ausbeute, Filtrationsverhalten, Qualitätsresultaten und Zuverlässigkeit im kommerziellen Maßstab.
Warum wurde unsere Ficin-Hydrolyse-Charge bitter oder zu dünn?
Bitterkeit oder ein übermäßiger Viskositätsverlust deuten häufig auf Überhydrolyse, zu hohe Dosierung, lange Verweilzeit, erhöhte Temperatur oder eine verzögerte Inaktivierung hin. Prüfen Sie Zeitpunktsproben, Endpunktdaten und Dosieraufzeichnungen. Ein Korrekturversuch kann die Enzymmenge reduzieren, die Haltezeit verkürzen, die Temperatur senken oder den Stopp-Schritt straffen. Sensorische Prüfungen und Peptidprofil-Analysen können helfen, das akzeptable Betriebsfenster zu bestimmen.
Verwandt: Ficin-Enzym-Anwendungen für industrielle Proteolyse
Machen Sie aus diesem Leitfaden eine Lieferantenanfrage Fordern Sie COA, TDS, SDS und eine Pilotprobe von Ficin für die Validierung der Proteinhydrolyse an. Sehen Sie sich unsere Anwendungsseite zu Ficin-Enzym-Anwendungen für industrielle Proteolyse unter /applications/ficin-enzyme-uses/ für Spezifikationen, MOQ und eine kostenlose 50 g Probe an.
Contact Us to Contribute